hacer un blog sobre el modelo atómico den rut5herford
 Antes de que Rutherford propusiera su modelo atómico, los físicos aceptaban que las cargas eléctricas en el átomo tenían una distribución más o menos uniforme. Rutherford trató de ver cómo era la dispersión de las partículas alfa
por parte de los átomos de una lámina de oro muy delgada. Los ángulos
resultantes de la desviación de las partículas supuestamente aportarían
información sobre cómo era la distribución de carga en los átomos. Era
de esperar que, si las cargas estaban distribuidas uniformemente según
el modelo atómico de Thomson,
la mayoría de las partículas atravesarían la delgada lámina sufriendo
solo ligerísimas deflexiones, siguiendo una trayectoria aproximadamente
recta. Aunque esto era cierto para la mayoría de las partículas alfa, un
número importante de estas sufrían deflexiones de cerca de 180º, es
decir, prácticamente salían rebotadas en dirección opuesta a la
incidente.
Antes de que Rutherford propusiera su modelo atómico, los físicos aceptaban que las cargas eléctricas en el átomo tenían una distribución más o menos uniforme. Rutherford trató de ver cómo era la dispersión de las partículas alfa
por parte de los átomos de una lámina de oro muy delgada. Los ángulos
resultantes de la desviación de las partículas supuestamente aportarían
información sobre cómo era la distribución de carga en los átomos. Era
de esperar que, si las cargas estaban distribuidas uniformemente según
el modelo atómico de Thomson,
la mayoría de las partículas atravesarían la delgada lámina sufriendo
solo ligerísimas deflexiones, siguiendo una trayectoria aproximadamente
recta. Aunque esto era cierto para la mayoría de las partículas alfa, un
número importante de estas sufrían deflexiones de cerca de 180º, es
decir, prácticamente salían rebotadas en dirección opuesta a la
incidente.Rutherford pensó que esta fracción de partículas rebotadas en dirección opuesta podía ser explicada si se suponía la existencia de fuertes concentraciones de carga positiva en el átomo. La mecánica newtoniana en conjunción con la ley de Coulomb predice que el ángulo de deflexión de una partícula alfa relativamente liviana por parte de un átomo de oro más pesado, depende del "parámetro de impacto" o distancia entre la trayectoria de la partícula y el núcleo:
- Por un lado se planteó el problema de cómo un conjunto de cargas positivas podían mantenerse unidas en un volumen tan pequeño, hecho que llevó posteriormente a la postulación y descubrimiento de la fuerza nuclear fuerte, que es una de las cuatro interacciones fundamentales.
- Por otro lado existía otra dificultad proveniente de la electrodinámica
clásica que predice que una partícula cargada y acelerada, como sería
el caso de los electrones orbitando alrededor del núcleo, produciría radiación electromagnética, perdiendo energía y finalmente cayendo sobre el núcleo. Las leyes de Newton, junto con las ecuaciones de Maxwell del electromagnetismo aplicadas al átomo de Rutherford llevan a que en un tiempo del orden de
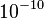 s, toda la energía del átomo se habría radiado, con la consiguiente caída de los electrones sobre el núcleo.2 Se trata, por tanto de un modelo físicamente inestable, desde el punto de vista de la física clásica.
s, toda la energía del átomo se habría radiado, con la consiguiente caída de los electrones sobre el núcleo.2 Se trata, por tanto de un modelo físicamente inestable, desde el punto de vista de la física clásica.

No hay comentarios:
Publicar un comentario